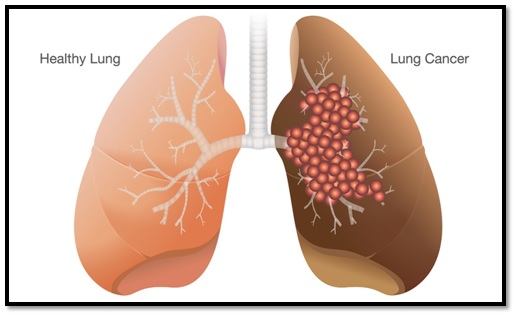
FDA ให้การรับรอง Enhertu สำหรับใช้รักษาผู้ป่วย unresectable หรือ metastatic non-small cell lung cancer (NSCLC) อายุตั้งแต่ 18 ปีขึ้นไป ที่ tumors มี activating HER2 (ERBB2) mutations โดย Enhertu ถือเป็น HER2-directed antibody drug conjugate (ADC) ตัวแรกที่ได้รับการรับรองจาก FDA ด้วยข้อบ่งใช้ดังกล่าว
เมื่อวันที่ 12 สิงหาคม 2565 AstraZeneca และ Daiichi Sankyo แจ้งว่า สำนักงานอาหารและยาของสหรัฐอเมริกา (Food and Drug Administration) หรือ FDA ได้ให้การรับรอง Enhertu (trastuzumab deruxtecan) ซึ่งเป็น HER2-directed antibody drug conjugate (ADC) สำหรับใช้ในการรักษาผู้ป่วย unresectable หรือ metastatic non-small cell lung cancer (NSCLC) อายุตั้งแต่ 18 ปีขึ้นไป ที่ tumors มี activating HER2 (ERBB2) mutations และผ่านการรักษาด้วย systemic therapy มาก่อนแล้ว โดยขนาดของ trastuzumab deruxtecan ที่ได้รับการรับรองในข้อบ่งใช้นี้ก็คือ 5.4 mg/k (intravenous infusion
ดร.นพ. Bob T. Li แพทย์ผู้เชี่ยวชาญทางด้านมะเร็งวิทยาของ Memorial Sloan Kettering Cancer Center (MSK) ในนครนิวยอร์กของสหรัฐอเมริกา กล่าวว่า การที่ FDA ให้การรับรอง trastuzumab deruxtecan ในข้อบ่งใช้สำหรับมะเร็งปอดชนิด NSCLC คือหลักชัยที่สำคัญสำหรับผู้ป่วยและประชาคมแพทย์ผู้เชี่ยวชาญทางด้านมะเร็งวิทยา โดยหลังจาก 2 ทศวรรษของการศึกษาวิจัยเกี่ยวกับบทบาทของการรักษาที่พุ่งเป้าไปที่ HER2 ในมะเร็งปอด การให้การรับรองของ FDA ที่มีต่อ HER2-directed antibody drug conjugate ตัวแรกนั่นก็คือ trastuzumab deruxtecan เท่ากับเป็นการยืนยันว่า HER2 เป็นเป้าหมายหนึ่งที่สามารถจัดการได้ในมะเร็งปอด และถือเป็นความก้าวหน้าที่สำคัญสำหรับการรักษาประชากรผู้ป่วยมะเร็งปอดชนิด NSCLC ที่มี HER2 mutations
ขณะที่ ดร. Upal Basu Roy ผู้อำนวยการด้านงานวิจัยของ LUNGevity Foundation องค์กรไม่แสวงหาผลกำไรที่มุ่งให้การสนับสนุนและส่งเสริมการศึกษาวิจัยและการให้ความรู้เพื่อช่วยให้ผู้ป่วยมะเร็งปอดมีผลลัพธ์ที่ดีขึ้น กล่าวว่า การที่ FDA อนุมัติ trastuzumab deruxtecan ออกมาใช้ในฐานะเป็น HER2 targeted treatment option ตัวแรก ถือเป็นข่าวที่ยิ่งใหญ่สำหรับผู้ป่วยมะเร็งปอดชนิด NSCLC ที่มี HER2 mutations
อนึ่ง จากข้อมูลขององค์การอนามัยโลกที่รายงานไว้ในเดือนสิงหาคม ปี 2020 พบว่า มะเร็งปอดเป็นโรคมะเร็งที่พบได้บ่อยเป็นอันดับ 2 ของโรคมะเร็งต่าง ๆ ทั่วโลก โดยมีผู้ที่ได้รับการวินิจฉัยว่าเป็นมะเร็งปอดจำนวนมากกว่า 2 ล้านคนทั่วโลก ในปี 2020 ซึ่งราว ๆ 80-85% ของมะเร็งปอดจัดเป็นมะเร็งชนิด NSCLC และในจำนวนนี้มีที่เป็น HER2 mutated NSCLC อยู่ประมาณ 2-4% โดยก่อนหน้าที่ trastuzumab deruxtecan จะได้รับการรับรองจาก FDA สำหรับมะเร็งปอดชนิด NSCLC ที่มี HER2 mutations นั้น ยังไม่มียาตัวใดที่ได้รับการรับรองจาก FDA โดยเฉพาะสำหรับผู้ป่วยมะเร็งปอดชนิด NSCLC ที่มี HER2 mutations
สำหรับข้อมูลด้านประสิทธิภาพและความปลอดภัยที่สำคัญที่นำมาสู่การได้รับการรับรองของ trastuzumab deruxtecan จาก FDA ก็คือ ผลลัพธ์จากการศึกษาทางคลินิกที่มีชื่อว่า DESTINY-Lung02 ซึ่งเป็นการศึกษาแบบ randomized, two-arm, phase 2, multicenter study ที่เปรียบเทียบระหว่างการให้ trastuzumab deruxtecan 6.4 mg/kg และ 5.4 mg/kg (intravenous infusion every 3 weeks) ในผู้ป่วย unresectable หรือ metastatic NSCLC ที่ tumors มี HER2 mutations จำนวนประมาณ 150 คน ที่มี disease recurrence หรือ progression ในระหว่างหรือหลังจากได้รับการรักษาด้วย prior anticancer therapy (second line or later) อย่างน้อย 1 regimen ที่ต้องมี platinum-based chemotherapy drug ร่วมอยู่ด้วย
DESTINY-Lung02 มี primary endpoint อยู่ที่ objective response rate (ORR) ที่ประเมินโดย blinded independent central review ขณะที่ secondary endpoints ได้แก่ disease control rate, duration of response (DoR), progression-free survival (PFS), investigator-assessed ORR, overall survival (OS), pharmacokinetics, time to response, quality of life และ safety
ผลการศึกษาที่เป็น interim efficacy analysis ใน pre-specified patient cohort พบว่า กลุ่มผู้ป่วยที่ได้รับ trastuzumab deruxtecan 5.4 mg/kg มี confirmed ORR อยู่ที่ 57.7% (52 คน; 95% confidence interval [CI] 43.2-71.3) ขณะเดียวกันพบว่ามี complete responses (CR) อยู่ที่ 1.9% และมี partial responses (PR) อยู่ที่ 55.8% ด้วย DoR ที่ 8.7 เดือน (95% CI 7.1-NE) ส่วนข้อมูลด้านความปลอดภัยโดยรวมจากการประเมินผู้ป่วย 101 คน ที่ได้รับ trastuzumab deruxtecan 5.4 mg/kg พบว่ามี safety profile ไม่แตกต่างจากการศึกษาทางคลินิกก่อนหน้านี้ โดยไม่มี safety concerns ใหม่ ๆ เกิดขึ้นเลย
ส่วน companion diagnostic test ที่ FDA ให้การรับรองสำหรับใช้ในการคัดเลือกผู้ป่วย unresectable หรือ metastatic NSCLC ที่ tumors มี HER2 mutations เพื่อนำเข้าสู่การรักษาด้วย trastuzumab deruxtecan ก็คือ Guardant360 CDx liquid biopsy test ของบริษัท Guardant Health
นอกจาก DESTINY-Lung02 trial แล้ว ยังมีอีก 1 การศึกษาทางคลินิกที่สำคัญของ trastuzumab deruxtecan ในผู้ป่วย unresectable หรือ metastatic NSCLC ที่ tumors มี HER2 mutations นั่นก็คือ การศึกษาที่มีชื่อว่า DESTINY-Lung01 ซึ่งเป็นการศึกษาแบบ global Phase II, open-label, two-cohort trial ที่ประเมินประสิทธิภาพและความปลอดภัยของ trastuzumab deruxtecan ในผู้ป่วย unresectable หรือ metastatic NSCLC ที่ tumors มี HER2 mutations (ได้รับ trastuzumab deruxtecan 6.4 mg/kg) หรือผู้ป่วย unresectable หรือ metastatic NSCLC ที่มี HER2-overexpressing (defined as IHC 3+ or IHC 2+) [ได้รับ trastuzumab deruxtecan 6.4 mg/kg และ 5.4 mg/kg] จำนวนทั้งสิ้น 91 คน
ผลการศึกษาของ DESTINY-Lung01 trial ที่เพิ่งได้รับการตีพิมพ์ในวารสารการแพทย์ New England Journal of Medicine (NEJM) เมื่อเดือนมกราคม ปี 2022 นี้ จากการติดตามผู้ป่วยเป็นเวลาเฉลี่ย 13.1 เดือน พบว่า กลุ่มผู้ป่วยที่ได้รับ trastuzumab deruxtecan 6.4 mg/kg มี ORR ซึ่งเป็น primary endpoint ของการศึกษานี้เช่นกัน อยู่ที่ 54.9% (95% CI 44.2-65.4), มีผู้ป่วย 1 คน (1.1%) ที่มี complete response และมีผู้ป่วย 49 คน (53.8%) ที่มี partial response ขณะเดียวกันพบว่ามี confirmed disease control rate (DCR) อยู่ที่ 92.3% และผู้ป่วยส่วนใหญ่มี tumor size ลดลงอย่างชัดเจน อีกทั้งยังพบว่ามี median DoR อยู่ที่ 9.3 เดือน, มี median PFS อยู่ที่ 8.2 เดือน และมี median OS อยู่ที่ 17.8 เดือน

สำหรับข้อมูลด้านความปลอดภัยโดยรวมของ trastuzumab deruxtecan ใน DESTINY-Lung01 trial พบว่า ผู้ป่วยทั้ง 91 คน มี adverse event เกิดขึ้นอย่างน้อย 1 อย่าง และผู้ป่วย 88 คน (97%) มี adverse event เกิดขึ้นอย่างน้อย 1 อย่าง ที่สัมพันธ์กับการได้รับ trastuzumab deruxtecan อย่างไรก็ตาม adverse events ที่เกิดขึ้นในผู้ป่วยตั้งแต่ 20% ขึ้นไป ส่วนใหญ่เป็น grade 1 หรือ 2 adverse events ซึ่งที่พบได้บ่อย ได้แก่ gastrointestinal และ hematologic events, decreased appetite และ alopecia
ในบทบรรณาธิการเกี่ยวกับ HER2-mutant NSCLC ในวารสาร NEJM ฉบับวันที่ 20 มกราคม 2565 ที่เขียนโดย นพ. Antonio Passaro (European Institute of Oncology IRCCS ในเมือง Milan ของอิตาลี) และ พญ. Solange Peters (Lausanne UniversityHospital ใน Switzerland) ระบุว่า ผลการศึกษาของ DESTINY-Lung01 trial สร้างมาตรฐานใหม่ของการรักษาสำหรับผู้ป่วยมะเร็งปอดชนิด non-small cell lung cancer ที่มี HER2 mutationsและดูเหมือนว่า trastuzumab deruxtecan จะมีศักยภาพที่แข็งแกร่งสำหรับผู้ป่วย HER2-mutated metastatic NSCLC ที่ยังไม่เคยได้รับการรักษาด้วย systemic therapy มาก่อน
นอกเหนือจาก trastuzumab deruxtecan จะได้รับการรับรองจาก FDA ในข้อบ่งใช้สำหรับผู้ป่วย unresectable หรือ metastatic NSCLC ที่ tumors มี HER2 mutations แล้ว เมื่อวันที่ 6 สิงหาคม 2565 AstraZeneca และ Daiichi Sankyo แจ้งว่า FDA ได้ให้การรับรอง trastuzumab deruxtecan สำหรับใช้รักษาผู้ป่วย unresectable หรือ metastatic breast cancer อายุตั้งแต่ 18 ปีขึ้นไป ที่มี HER2-low (IHC 1+ or IHC 2+/ISH-) และผ่านการรักษาด้วยยาเคมีบำบัดใน metastatic setting มาแล้ว หรือมี disease recurrence เกิดขึ้นในระหว่างหรือภายใน 6 เดือน หลังจากเสร็จสิ้นการได้รับ adjuvant chemotherapy โดย trastuzumab deruxtecan ถือเป็น HER2-directed therapy ตัวแรกที่ได้รับการรับรองจาก FDA ด้วยข้อบ่งใช้สำหรับผู้ป่วย HER2-low metastatic breast cancer
การศึกษาทางคลินิกที่มีชื่อว่า DESTINY-Breast04 ถือเป็นการศึกษาแรกที่ประเมินประสิทธิภาพและความปลอดภัยของ trastuzumab deruxtecan ซึ่งเป็น HER2-directed antibody drug conjugate (ADC) ในผู้ป่วย HER2-low (IHC 1+ or IHC 2+/ISH-) metastatic breast cancer โดยเป็นการศึกษาแบบ global, randomized, open-label, registrational Phase III trial เปรียบเทียบระหว่าง trastuzumab deruxtecan (5.4 mg/kg) และ physician’s choice of chemotherapy (capecitabine, eribulin, gemcitabine, paclitaxel หรือ nab-paclitaxel) ในผู้ป่วย HER2-low unresectable and/or metastatic breast cancer จำนวน 540 ราย ซึ่งส่วนใหญ่ (480 ราย) มี hormone receptor status เป็นบวก (HR-positive) และผ่านการรักษาด้วยยาเคมีบำบัดมาแล้วอย่างน้อย 1-2 ด่าน ผลการศึกษาพบว่า trastuzumab deruxtecan ลด risk of disease progression หรือ death ลงได้ถึง 50% เมื่อเทียบกับ physician’s choice of chemotherapy โดยกลุ่มผู้ป่วยที่ได้รับ trastuzumab deruxtecan มี median PFS อยู่ที่ 9.9 เดือน เทียบกับ 5.1 เดือน ของกลุ่มผู้ป่วยที่ได้รับ physician’s choice of chemotherapy ซึ่งแตกต่างกันอย่างมีนัยสำคัญทางสถิติ (hazard ratio [HR] 0.50; 95% confidence interval [CI] 0.40-0.63; p < 0.0001) ขณะเดียวกันพบว่ากลุ่มผู้ป่วยที่ได้รับ trastuzumab deruxtecan มี median OS อยู่ที่ 23.4 เดือน เทียบกับ 16.8 เดือน ซึ่งเท่ากับว่า trastuzumab deruxtecan ลด risk of death ลงได้ถึง 36% เมื่อเทียบกับ physician’s choice of chemotherapy (HR 0.64; 95% CI 0.49-0.84; p = 0.001)
อีกทั้งก่อนหน้านี้เมื่อเดือนมกราคม ปี 2021 trastuzumab deruxtecan ยังได้รับการรับรองจาก FDA ในข้อบ่งใช้สำหรับรักษาผู้ป่วย locally advanced หรือ metastatic HER2-positive gastric หรือ gastroesophageal junction (GEJ) adenocarcinoma อายุตั้งแต่ 18 ปีขึ้นไป ที่เคยได้รับการรักษาด้วย trastuzumab-based regimen มาก่อนแล้ว โดยผลลัพธ์ของการศึกษาทางคลินิกที่มีชื่อว่า DESTINY-Gastric01 phase 2 trial ซึ่งเป็นการศึกษาแบบ registrational Phase II, open-label, multi-centre trial ที่ประเมินประสิทธิภาพและความปลอดภัยของ trastuzumab deruxtecan 6.4 mg/kg เปรียบเทียบกับ investigator’s choice of chemotherapy (paclitaxel or irinotecan monotherapy) ในผู้ป่วย HER2-expressing advanced gastric cancer or gastroesophageal junction adenocarcinoma (IHC3+ or IHC2+/ISH+) จำนวน 189 ราย ในญี่ปุ่นและเกาหลีใต้ ที่ผ่านการรักษาด้วยยาเคมีบำบัดมาแล้วอย่างน้อย 2 ด่าน ซึ่งรวมถึงผ่านการรักษาด้วย fluoropyrimidine (5-FU) และ platinum chemotherapy ร่วมกับ trastuzumab มาแล้ว
ผลการศึกษาของ DESTINY-Gastric01 trial พบว่ากลุ่มผู้ป่วยที่ได้รับ trastuzumab deruxtecan มี risk of death ลดลงถึง 41% เมื่อเทียบกับกลุ่มผู้ป่วยที่ได้รับ investigator’s choice of chemotherapy (HR of 0.59; 95% confidence interval [CI] 0.39-0.88; p = 0.0097) และพบว่ากลุ่มผู้ป่วยที่ได้รับ trastuzumab deruxtecan มี median OS อยู่ที่ 12.5 เดือน [95% CI 9.6-14.3] เทียบกับ 8.4 เดือน [95% CI 6.9-10.7] ของกลุ่มผู้ป่วยที่ได้รับ investigator’s choice of chemotherapy
ขอขอบคุณแหล่งที่มาของข้อมูล: www.healio.com, www.drugs.com, www.astrazeneca.com, www.nejm.org